Singapour : La HSA révise son système d'avis de modification des DM
有任何问题?向我们的专家获取相关信息
联系我们2015年 12月 10日
La Health Sciences Authority (HSA), réglementant le marché des dispositifs médicaux à Singapour, annonce des révisions de son système d'avis de modification pour les dispositifs médicaux, à compter du 1er décembre 2015.
 Une nouvelle directive de la HSA annonce plusieurs mises à jour qui, selon la HSA, rendront le processus de notification des modifications plus efficace et rationnel pour les dispositifs enregistrés. La notification des modifications implique que les fabricants doivent informer rapidement la HSA de tout changement ou modification apportés à leurs dispositifs afin de continuer à commercialiser légalement à Singapour.
Une nouvelle directive de la HSA annonce plusieurs mises à jour qui, selon la HSA, rendront le processus de notification des modifications plus efficace et rationnel pour les dispositifs enregistrés. La notification des modifications implique que les fabricants doivent informer rapidement la HSA de tout changement ou modification apportés à leurs dispositifs afin de continuer à commercialiser légalement à Singapour.
Les points importants de ces révisions de l'avis de modification :
- L'ajout d'un dispositif avec un nom de propriétaire différent à l'inventaire d'un dispositif enregistré ne rentrera pas dans le cadre d'un avis de modification mais nécessitera un nouvel enregistrement préalable à la commercialisation auprès de la HSA.
- L'ajout de nouveaux modèles à un dispositif va maintenant tomber dans la catégorie de modification d'examen (Review Change) du processus de gestion des modifications de la HSA.
- Dans les cas où les avis de modifications sont motivés par des effets indésirables ou des mesures correctives de sécurité lors de l'utilisation, les titulaires d'un enregistrement doivent fournir à la HSA les documents associés, tels que les avis relatifs à la sécurité, l'évaluation des risques pour la santé, l'analyse de la cause première et les mesures préventives et correctives.
- Après l'approbation par la HSA de l'avis de modification, un fabricant peut commercialiser à Singapour le dispositif original enregistré et celui modifié uniquement si les deux versions de son produit répondent aux exigences essentielles pour la sécurité et la performance.
La nouvelle directive fournit également un tableau indiquant plus clairement quelles classes de dispositifs médicaux font l'objet desquels des quatre types de notifications (avis) de modification (modifications techniques, modification d'examen, modifications administratives et/ou notifications) :
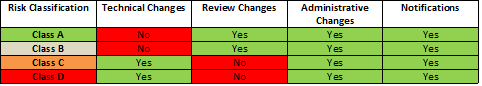
Les acteurs du marché singapourien concernés devraient consulter la nouvelle directive pour connaître la liste complète des révisions et déterminer si celles-ci, ou l'une d'entre elles, auront un impact sur leur activité.
Vous trouverez d'autres informations sur la marche à suivre pour l'enregistrement d'un dispositif médical à Singapour dans notre livre blanc et notre présentation vidéo.